Rozmawiam z dr hab. inż. Katarzyną Nawrotek z ICRI-BioM o projekcie „Biomateriały indukujące demetylację DNA jako narzędzia do przyszłych terapii regeneracji neuronów”, przyznanym przez NCN w konkursie OPUS 25.
Badania będą realizowane we współpracy z dr. Przemysławem Płocińskim z Katedry Immunologii i Biologii Infekcyjnej na Wydziale Biologii i Ochrony Środowiska Uniwersytetu Łódzkiego. W interdyscyplinarnym zespole są też naukowcy z zagranicy - dr Anika Nagelkerke z Groningen Research Institute of Pharmacy w Holandii oraz dr Ksenia Skvortsova z australijskiego The Garvan Institute of Medical Research.
W swoich badaniach zajmuje się Pani zagadnieniami regeneracji neuronów, dlaczego ten temat jest tak ważny?
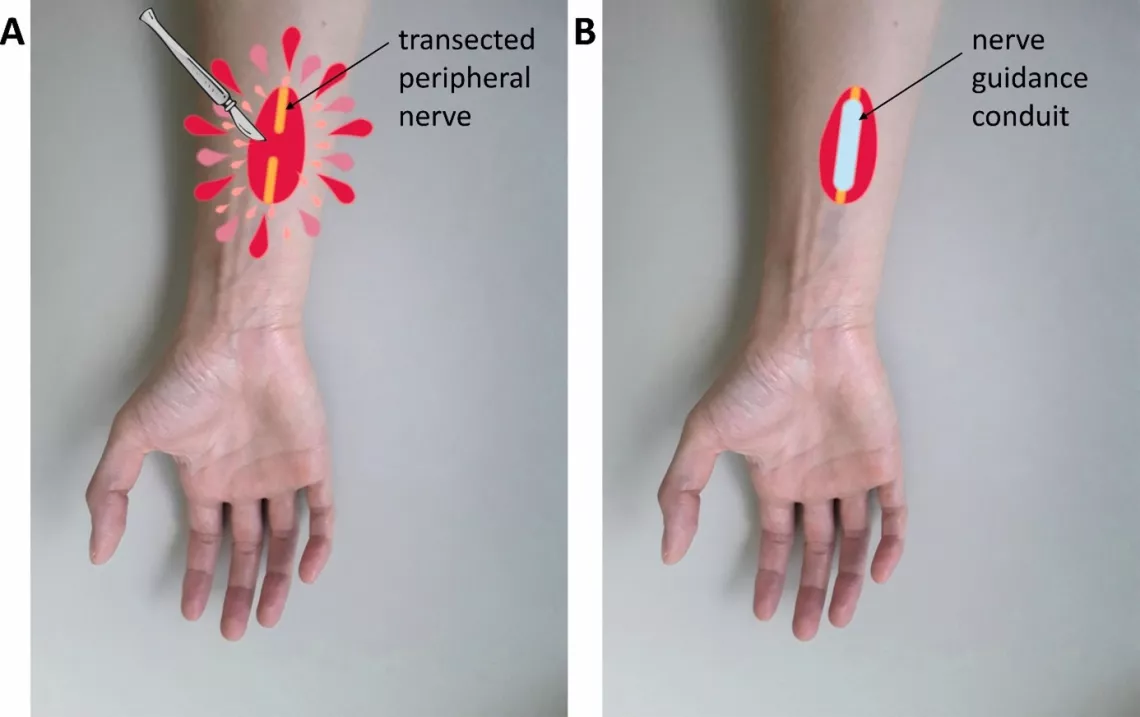
- Co roku rośnie liczba pacjentów cierpiących z powodu uszkodzeń nerwów. Niestety najczęściej całkowite odzyskanie utraconych funkcji sensorycznych i motorycznych po przecięciu nerwu obwodowego jest rzadko osiągane ze względu na złożoną budowę anatomiczną ludzkiego ciała i hamujące naprawę neuronów oddziaływanie środowiska zewnątrzkomórkowego tkanki nerwowej.
Jakie metody są stosowane do leczenia urazów nerwów obwodowych?
Można do nich zaliczyć zszycie nerwu „koniec do końca”, autotransplantację i przeszczep od obcego dawcy. W ostatnich dwóch dekadach badania koncentrowały się na zastąpieniu tych tradycyjnych sposobów leczenia przez metody wykorzystujące osiągnięcia inżynierii biomedycznej. Najbardziej obiecującym kierunkiem dla badaczy zajmujących się inżynierią tkankową i medycyną regeneracyjną jest projektowanie implantów nerwowych. Ostatnie postępy w biologii molekularnej i neurobiologii pomagają w odkryciu skutecznych narzędzi do regeneracji komórek nerwowych.
Czego można oczekiwać po projekcie, nad którym teraz Pani pracuje?
Planujemy opracować implant nerwowy zdolny do uwalniania cząsteczek, które indukują zmiany w ekspresji genów (jest to proces, dzięki któremu w komórkach naszego ciała powstają funkcjonalne produkty, głównie białka). Nas oczywiście najbardziej interesują te geny, które są krytyczne dla regeneracji neuronów. Ostatnie badania wskazują, że demetylacja DNA promowana przez dioksygenazy metylocytozyny, enzymy TET (z ang. Ten-eleven translocation methylcytosine dioxygenases) jest podstawowym mechanizmem przeprogramowywania statusu komórkowego dojrzałych neuronów ssaków w celu umożliwienia wzrostu włókien nerwowych.
Czy można jakoś prosto powiedzieć co to jest demetylacja DNA i dlaczego jest tak ważna?
Od poczęcia aż od śmierci w naszych komórkach zachodzi kontrolowana metylacja i demetylacja DNA, która ma m.in. regulować ekspresję konkretnych genów. Najprościej mówiąc, są to procesy wprowadzania drobnych modyfikacji pojedynczych, precyzyjnie wybranych „cegiełek” w łańcuchu naszej informacji genetycznej. Modyfikacje te są konieczne dla uruchamiania i wygaszania precyzyjnych programów komórkowych, decydujących o losie (m.in. potencjale regeneracyjnym) komórek budujących różne rodzaje tkanek. Demetylacja jest reakcją odwrotną metylacji, powodującą ponowne uruchomienie ekspresji pewnych grup genów. W celu zrozumienia mechanizmów sprzyjających skutecznej regeneracji aksonów obwodowych, przeprowadzimy kompleksowe badania zmian ekspresji genów po wprowadzeniu do hodowanych komórek nerwowych in vitro i modelu zwierzęcego in vivo biomateriałów indukujących demetylację DNA. Trzeba pamiętać, że istnieje wiele poziomów regulacji ekspresji genów i są to procesy niezwykle złożone.
Jakich efektów się Państwo spodziewacie?
Mamy nadzieję, że wyniki projektu pomogą, w perspektywie trudnej dziś do określenia, wskazać drogę do opracowania nowych metod terapeutycznych umożliwiających odzyskanie utraconych funkcji czuciowych i ruchowych po przecięciu nerwów obwodowych. W tym przekonaniu utwierdzają nas bardzo obiecujące wyniki badań wstępnych, które wraz z zespołem przeprowadziliśmy w fazie przygotowawczej, w ramach wcześniejszych projektów naukowych, kierowanych przeze mnie.